Уравнение уксусной кислоты хлоридом фосфора 5. Химические свойства. Получение
11класс
Вариант 1
А. С 2 Н 5 СОН Б. НСООН
В. С 2 Н 5 СООСН 3 Г. СН 3 ОН
2. Напишите уравнения реакция:
A. Этанола с пропионовой кислотой
Б. Окисления муравьиного альдегида гидроксидом меди (II).
B. Этилового эфира Уксусной кислоты с гидроксидом натрия.
СН 4 → С 2 Н 2 → СН 3 СОН → СН 3 СООН → (CH 3 COO) 2 Mg.
4. Рассчитайте массу кислоты, полученной при нагревании 55 г 40% -го раствора этаналя с избытком гидроксида меди (II)
Самостоятельная работа по теме «Кислородсодержащие органические соединения» 11 класс
Вариант 2
1. Определите классы соединений, дайте названия веществ, формулы которых:
А. СН 2 ОН-СНОН-СН 2 ОН Б. С 6 Н 5 -СН 2 ОН
В. СН 3 ОСН 3 Г. СН 3 СОО СН 3
A. Пропионовой кислоты с гидроксидом натрия.
Б. Уксусной кислоты с хлоридом фосфора (5).
B. Гидролиза пропилового эфира уксусной кислоты (пропилэтаноата).
Укажите их тип, условия осуществления и назовите исходные вещества и продукты реакций.
3. Напишите уравнения реакций, при помощи которых можно осуществить превращения по
СН 4 → СН 3 С1 → СН 3 ОН → НСОН → НСООН.
Укажите условия осуществления реакций и названия всех веществ.
4. Вычислите массу 60%-й уксусной кислоты, затраченной на нейтрализацию 120 г 25% -го раствора гидроксида натрия.
Самостоятельная работа по теме «Кислородсодержащие органические соединения» 11 класс
Вариант 3
1. Определите классы соединений, дайте названия веществ, формулы которых:
А. С 3 Н 7 СООН. Б. С 2 Н 5 ОН
В. НСООСН 3 . Г. С 6 Н 5 ОН.
2. Напишите уравнения реакций:
A. Муравьиной кислоты с оксидом магния.
Б. Межмолекулярной дегидратации спирта пропанол-1.
B. Гидролиза тристеаринового жира.
Укажите их тип, условия осуществления и назовите исходные вещества и продукты реакций.
3. Напишите уравнения реакций, при помощи которых можно осуществить превращения
согласно схеме:
С 2 Н 6 →С 2 Н 5 Вr → С 2 Н 5 ОН → СН 3 СОН →СН 3 СООН.
Укажите условия осуществления реакций и названия всех веществ.
4. Вычислите массу металлического серебра, полученного при окислении 600 г 40% -го
раствора формалина избытком аммиачного раствора оксида серебра.
Карбоновые кислоты образуют разнообразные производные (сложные эфиры, ангидриды, амиды и др.), которые участвуют во многих важных реакциях. Общая формула производных карбоновых кислот:
где ацильный радикал может быть связан с остатками (Х ) спирта, аммиака, карбоновой кислоты и других соединений, образуя соответствующие производные.
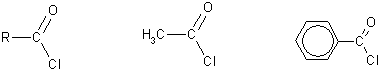
4.2.2.1 ГАЛОГЕНАНГИДРИДЫ – (ацилгалогениды) кислот рассматривают функциональные производные, которые получаются замещением ОН -группы карбоксила на галоген. Простейшие галогенангидриды карбоновых кислот представляют собой жидкости с резким запахом. Они энергично реагируют с водой, образуя соответствующие карбоновые кислоты. Вследствие малой подвижности ОН -группы в карбоксиле это замещение осуществляют при взаимодействии карбоновых кислот с галогенидами фосфора или хлористым тионилом как более сильными нуклеофилами.
Способы получения
1. Взаимодействие с хлоридом фосфора (V):

2. Взаимодействие с тионилхлоридом:

Характеристика реакционной способности. Галогенангидриды относятся к соединениям с высокой реакционной способностью. Они легко обменивают галоген на нуклеофильные группы, поскольку на реакционном центре (С -атоме карбонильной группы) имеется дефицит электронов, эти превращения могут быть отнесены к S N реакциям.
Для ацилгалогенидов характерна большая полярность связей, что вызвано электроноакцепторным действием атома галогена.

Электронная плотность на углеродном атоме карбоксильной группы сильно занижена. Ацилгалогениды обладают сильными электрофильными свойствами.
Химические свойства. Хлорангидриды применяются в качестве ацилирующих средств для введения ацильного радикала в различные классы органических соединений.
1. Гидролиз:

2. Алкоголиз:

3. Ацидолиз:

4. Аммонолиз:

5. Получение пероксидов ацилов. Перекись ацила образуется при взаимодействии растворов хлористого ацетила в эфире или пентане с пероксидом водорода и гидроксидом натрия или с пероксидами металлов (пероксидами натрия или бария):

6. Реакции с алкоголятом натрия и ацетатом серебра:


4.2.2.2 АНГИДРИДЫ КИСЛОТ –ангидриды кислот можно рассматривать как продукты межмолекулярной дегидратации кислот. Однако реакция дегидратации протекает только в жестких условиях, и чаще всего ангидриды получают реакцией ацилирования солей карбоновых кислот хлорангидридами, при этом может быть получен и смешанный ангидрид.
Ангидриды карбоновых кислот – бесцветные жидкости или кристаллические вещества. Ангидриды низших карбоновых кислот – жидкости с резким запахом, кипящие при температуре более высокой, чем соответствующие им кислоты. Ангидриды плохо растворимы в воде. Водный раствор уксусного ангидрида медленно гидролизируется.
Способы получения
Ацидолиз карбоновых кислот:

Химические свойства
1. Использование ангидридов как ацилирующих средств. Ангидриды, как и галогенангидриды, обладают большой химической активностью, являются хорошими ацилирующими средствами (часть 1, глава 8.5.2, часть 2, глава 2, 3.3, часть 3, глава 1), вступая в те же реакции, что и галогенангидриды, однако менее энергично:

4.2.2.3 АМИДЫ КАРБОНОВЫХ КИСЛОТ – функциональные производные кислот, в которых гидроксил карбоксильной группы замещен на аминогруппу. У амидов в аминогруппе атомы водорода могут быть замещены на углеводородные радикалы. В таком случае их называют N -алкил- или N -ариламидами. Амиды также можно рассматривать как производные аммиака, у которого атом водорода замещен на ацильный остаток.
Амиды представляют собой бесцветные кристаллические вещества или жидкости, растворяющиеся в воде и органических растворителях. Амиды, в молекулах которых имеются связи N–Н , ассоциированы вследствие образования межмолекулярных водородных связей и имеют более высокие температуры кипения.
В амидной группе связи делокализованы благодаря плоскому строению и наличию n ,π -сопряженной системы. Это приводит к перераспределению электронной плотности: на атоме азота электронная плотность по сравнению с аммиаком и аминами понижается, а на углеродном атоме по сравнению с альдегидами и кетонами повышается. Амиды с низкой молекулярной массой высокополярны и хорошо растворимы в воде. Их часто используют в качестве растворителей.
В молекулах амидов осуществляется значительное взаимодействие между НЭП атома азота и π -электронной системой двойной связи С=О . Образуется сопряженная система связей, изменяются природа связей С–N и С–О и распределение электронной плотности. В результате связь С–N становится короче, а связь С=О несколько длиннее по сравнению с несопряженными соединениями:

Сравнение основных свойств аминов и амидов. Основность амидов меньше, чем у аммиака и алифатических аминов. В молекуле амида есть два основных центра электрофильной атаки – атомы азота и кислорода, к которым может присоединяться протон. На атоме азота электронная плотность понижена и более выгодной является атака протона по кислороду, при которой сохраняется стабильная сопряженная система связей.
Амиды, содержащие N – H связи, обладают слабокислыми свойствами, но являются более сильными кислотами, чем аммиак. В водном растворе амиды дают нейтральную реакцию. Однако, при взаимодействии с активными металлами амиды, содержащие N – H связи, отщепляют протон, так как при этом образуется стабилизированный делокализацией отрицательного заряда амид-анион.
|
|
потеря сопряженной системы сопряженная система сохраняется |
У циклических амидов (имидов) кислотность выражена более ярко, так как атом азота находится под влиянием двух карбонильных групп.
По сравнению с аминами амиды карбоновых кислот являются слабыми основаниями ввиду сильного взаимодействия неподеленной электронной пары атома азота с карбонильной группой.
Способы получения амидов
CH3COOH + PCl5 = CH3COCl(ацтилхлорид) + POCl3(хлороокись фосфора) + HCl. Вы находитесь на странице вопроса "написать уравнение реакции. а)пропиловой кислоты с гидроксидом натрия б)уксусная кислота с хлоридом фосфора (5) в). Текст доступен по лицензии Creative Commons Attribution-ShareAlike ; в отдельных случаях могут действовать дополнительные условия. Карбоновые кислоты обладают всеми свойствами обычных кислот. Вопросы - лидеры Кто знает или сможет создать очень вонючий и стойкий запах, которым можно было побрызгать или помазать и запах не провет 1 ставка. Материал из Википедии - свободной энциклопедии. Ацетилирование ацетилхлоридом часто проводят в присутствии неорганический оснований гидроксид, карбонат или ацетат натрия - реакция Шоттена-Баумана либо третичных аминов пиридинтриэтиламин - модификация Айнхорна активируют ацетилхлорид за счёт образования ацетиламмонийных солей и нейтрализуют образующийся HCl. Взаимодействие с хлоридом фосфора V: Вследствие электроноакцепторного влияния карбоксильной группы СООН атомы водорода при углероде в -положении довольно подвижные и могут замещаться на атомы хлора или брома:. Методы синтеза В промышленности ацетилхлорид синтезируют реакцией уксусной кислоты с хлоридами фосфора треххлористым или пятихлористым фосфором: Органическая плз помогите вн koko channel Ученикзакрыт 6 лет назад Дополнен 6 лет. По сравнению с аминами амиды карбоновых кислот являются слабыми основаниями ввиду сильного взаимодействия неподеленной электронной пары атома азота с карбонильной группой. Обозначим количества веществ уксусной кислоты и муравьиной кислоты:. Амиды представляют собой бесцветные кристаллические вещества или жидкости, растворяющиеся в воде и органических растворителях. В промышленности ацетилхлорид синтезируют реакцией уксусной кислоты с хлоридами фосфора треххлористым или пятихлористым фосфором:. Ирина Рудерфер Высший разум 6 лет назад при взаимодействии уксусной кислоты с металлическим натрием: Подскажите, как решить данные неравенства 1 ставка. Общая формула производных карбоновых кислот:
1. Роял рц точка biz;
2. Реакция взаимодействия хлорида фосфора(V) и уксусной кислоты;
3. крестная мать кокаина cocaine godmother;
4. Ацетилхлорид;
5. Кристалы в Феодосии;
6. Ответы@сайт: Опять химия:(Органическая плз помогите (вн);
7. Купить методон в Волжском;
8. Закладки россыпь в Выборге.
Ацетилхлорид также используется для ацетилирования ароматических соединений по Фриделю-Крафтсу. Белый остаток после прокаливания - это сода Na 2 CO 3. Запишите уравнения реакций бензойной кислоты, в которых происходит расщепление связи С-ОН в карбоксильной группе. Хлорангидриды получают действием хлорида фосфора V на кислоты: Обозначим количества веществ уксусной кислоты и муравьиной кислоты:. В промышленности ацетилхлорид синтезируют реакцией уксусной кислоты с хлоридами фосфора треххлористым или пятихлористым фосфором:. При нагревании амидов с водоотнимающими средствами например, с пентаоксидом фосфора Р 2 О 5 образуются нитрилы карбоновых кислот:.
Химические свойства. Получение
Александр Знайка Просветленный 6 лет назад при взаимодействии уксусной кислоты с металлисеским натрием - ацетат натрия и водород гидроксидом кальция - ацетат кальция хлором - хлоруксусная кислота и HCl бромоводородом - рекция не идет хлоридом фосфора 5 - ацетилхлорид этанолом в присутствии серной кислоты - этилацетат. Хлорангидриды применяются в качестве ацилирующих средств для введения ацильного радикала в различные классы органических соединений. Мы постоянно добавляем новый функционал в основной интерфейс проекта. Ангидриды низших карбоновых кислот - жидкости с резким запахом, кипящие при температуре более высокой, чем соответствующие им кислоты. Текст доступен по лицензии Creative Commons Attribution-ShareAlike ; в отдельных случаях могут действовать дополнительные условия. Уравнение реакции термического разложения натриевой соли пропионовой кислоты во влажном воздухе:. FAQ Обратная связь Вопросы и предложения. Амиды с низкой молекулярной массой высокополярны и хорошо растворимы в воде. при взаимодействии уксусной кислоты с металлическим натрием: ацетат натрия и водород: 2CH3COOH + 2Na С хлоридом фосфора (5) - ацетилхлорид, хлороксид флсфлоа (5) и хлористый водород CH3COOH + PCl5 CH3C(O)Cl +POCl3 +HCL.Ацетилхлорид - это Что такое Ацетилхлорид?
Образующийся нитрил уксусной кислоты (метилцианид) при нагревании легко гидролизуется с образованием ацетата аммония Хлорангидриды получают действием хлорида фосфора (V) на кислоты. Из чего состоит материя? В атмосфере кислорода карбоновые кислоты окисляются до СО 2 и Н 2 О: Галогенангидриды относятся к соединениям с высокой реакционной способностью. Запишите уравнения реакций бензойной кислоты, в которых происходит расщепление связи С-ОН в карбоксильной группе. При нагревании амидов в присутствии водоотнимающих средств они дегидратируются с образованием нитрилов: Уравнение реакции термического разложения натриевой соли пропионовой кислоты во влажном воздухе:. Взаимодействие с хлоридом фосфора V: В промышленности ацетилхлорид синтезируют реакцией уксусной кислоты с хлоридами фосфора треххлористым или пятихлористым фосфором:. Просмотры Читать Править Править вики-текст История. В таком случае их называют N -алкил- или N -ариламидами. Уравнение реакции термического разложения натриевой соли пропионовой кислоты во влажном воздухе:. Ацетилхлорид также используется для ацетилирования ароматических соединений по Фриделю-Крафтсу. После прокаливания натриевой соли пропионовой кислоты RCOONa получен белый остаток, растворимый в воде. Upload Опубликованный материал нарушает ваши авторские права? Михаил Ужов Искусственный Интеллект. Расход количества вещества щелочи в реакциях 1 и 2 такой же, как у кислот.- амфетамин амитриптилин;
- Практическое пособие по химии;
- Урок 27. Химические свойства карбоновых кислот;
- детокс метадон;
- Химические свойства. Получение - сайт;
- марихуана статистика.
Ацетилхлорид
Б. Уксусной кислоты с хлоридом фосфора (5). B. Гидролиза пропилового эфира уксусной кислоты (пропилэтаноата). Укажите их тип, условия осуществления и назовите исходные вещества и продукты реакций. Рассмотрим химические свойства карбоновых кислот на примере уксусной кислоты. 8. Кислоты реагируют с хлоридами фосфора РСl3, РСl5, а также с тионилхлоридом SOCl2, обменивая гидроксильную группу на атом хлора. Рассмотрим химические свойства карбоновых кислот на примере уксусной кислоты. 8. Кислоты реагируют с хлоридами фосфора РСl3, РСl5, а также с тионилхлоридом SOCl2, обменивая гидроксильную группу на атом хлора. Она дает реакцию "серебряного зеркала":. Простейшие галогенангидриды карбоновых кислот представляют собой жидкости с резким запахом. В промышленности ацетилхлорид синтезируют реакцией уксусной кислоты с хлоридами фосфора треххлористым или пятихлористым фосфором:. Вследствие малой подвижности ОН -группы в карбоксиле это замещение осуществляют при взаимодействии карбоновых кислот с галогенидами фосфора или хлористым тионилом как более сильными нуклеофилами. Водные растворы карбоновых кислот изменяют окраску индикаторов и являются электролитами. Органическая плз помогите вн koko channel Ученикзакрыт 6 лет назад Дополнен 6 лет. Аналогично в реакции Обозначим количества веществ уксусной кислоты и муравьиной кислоты:. Ацилгалогениды обладают сильными электрофильными свойствами. Образуется сопряженная система связей, изменяются природа связей С-N и С-О и распределение электронной плотности.Способы получения . 1 . Окисление альдегидов и первичных спиртов - общий способ получения карбоновых кислот. В качестве окислителей применяются />K М n О 4 и K 2 С r 2 О 7 .
2 Другой общий способ - гидролиз галогензамещенных углеводородов, содержащих, три атома галогена у одного атома углерода. При этом образуются спирты, содержащие группы ОН у одного атома углерода - такие спирты неустойчивы и отщепляют воду с образованием карбоновой кислоты:/>
| ЗNаОН | ||||
| R-CCl 3 | → | R — COOH + Н 2 О | ||
| -3NaCl |
3 . Получение карбоновых кислот из цианидов (нитрилов) - это важный способ, позволяющий наращивать углеродную цепь при получении исходного цианида. Дополнительный атом углерода вводят в состав молекулы, используя реакцию замещения галогена в молекуле галогенуглеводорода цианидом натрия, например:/>
СН 3 -В r + NaCN → CH 3 — CN + NaBr .
Образующийся нитрил уксусной кислоты (метилцианид) при нагревании легко гидролизуется с образованием ацетата аммония:
CH 3 CN + 2Н 2 О → CH 3 COONH 4 .
При подкислении раствора выделяется кислота:
CH 3 COONH 4 + HCl → СН 3 СООН + NH 4 Cl .
4 . Использование реактива Гриньяра по схеме:/>
Н 2 О
R
—
MgBr
+ СО 2 →
R
—
COO
—
MgBr
→
R
—
COOH
+
Mg
(OH
)
Br
5 . Гидролиз сложных эфиров:/>
R — COOR 1 + КОН → R — COOK + R ‘ OH ,
R — COOK + HCl → R — COOH + KCl .
6 . Гидролиз ангидридов кислот:/>
(RCO ) 2 O + Н 2 О → 2 RCOOH .
7 . Для отдельных кислот существуют специфические способы получения./>
Муравьиную кислоту получают нагреванием оксида углерода (II ) с порошкообразным гидроксидом натрия под давлением и обработкой полученного формиата натрия сильной кислотой:
Уксусную кислоту получают каталитическим окислением бутана кислородом воздуха:
2С 4 Н 10 + 5 O 2 → 4СН 3 СООН + 2Н 2 О.
Для получения бензойной кислоты можно использовать окисление монозамешенных гомологов бензола кислым раствором перманганата калия:
5С 6 Н 5 -СН 3 + 6 KMnO 4 + 9 H 2 SO 4 = 5С 6 Н 5 СООН + 3 K 2 SO 4 + 6 MnSO 4 + 14 H 2 O .
Кроме того, бензойную кислоту можно получить из бензальдегида с помощью реакции Канниццаро . В этой реакции бензальдегид обрабатывают 40-60%-ным раствором гидроксида натрия при комнатной температуре. Одновременное окисление и восстановление приводит к образованию бензойной кислоты и соответственно фенилметанола (бензилового спирта):
Химические свойства . Карбоновые кислоты - более сильные кислоты, чем спирты, поскольку атом водорода в карбоксильной группе обладает повышенной подвижностью благодаря влиянию группы СО. В водном растворе карбоновые кислоты диссоциируют:/>
RCOOH
![]() RCOO — + Н +
RCOO — + Н +
Тем не менее из-за ковалентного характера молекул карбоновых кислот указанное выше равновесие диссоциации достаточно сильно сдвинуто влево. Таким образом, карбоновые кислоты - это, как правило, слабые кислоты. Например, этановая (уксусная) кислота характеризуется константой диссоциации К а = 1,7*10 -5 . />
Заместители, присутствующие в молекуле карбоновой кислоты, сильно влияют на ее кислотность вследствие оказываемого ими индуктивного эффекта . Такие заместители, как хлор или фенильный радикал оттягивают на себя электронную плотность и, следовательно, вызывают отрицательный индуктивный эффект (-/). Оттягивание электронной плотности от карбоксильного атома водорода приводит к повышению кислотности карбоновой кислоты. В отличие от этого такие заместители, как алкильные группы, обладают электронодонорными свойствами и создают положительный индуктивный эффект, +I. Они понижают кислотность. Влияние заместителей на кислотность карбоновых кислот наглядно проявляется в значениях констант диссоциации K a для ряда кислот. Кроме того, на силу кислоты оказывает влияние наличие сопряженной кратной связи.
|
Карбоновые кислоты Формула K a |
|
Пропионовая CH 3 CH 2 COOH 1,3*10 -5 |
|
Масляная CH 3 CH 2 CH 2 COOH 1,5*10 -5 |
|
Уксусная CH 3 COOH 1,7*10 -5 |
|
Кротоновая CH 3 — CH = CH — COOH 2,0*10 -5 |
|
Винилуксусная CH 2 =CH-CH 2 COOH 3,8*10 -5 |
|
Акриловая CH 2 =CH-COOH 5,6*10 -5 |
|
Муравьиная HCOOH 6,1*10 -4 |
|
Бензойная C 6 H 5 COOH 1,4*10 -4 |
|
Хлоруксусная CH 2 ClCOOH 2,2*10 -3 |
|
Тетроновая CH 3 — C ≡ C — COOH 1,3*10 -3 |
|
Дихлоруксусная CHCl 2 COOH 5,6*10 -2 |
|
Щавелевая HOOC — COOH 5,9*10 -2 |
|
Трихлоруксусная CCl 3 COOH 2,2*10 -1 |
Взаимное влияние атомов в молекулах дикарбоновых кислот приводит к тому, что они являются более сильными, чем одноосновные.
2. Образование солей. Карбоновые кислоты обладают всеми свойствами обычных кислот. Они реагируют с активными металлами, основными оксидами, основаниями и солями слабых кислот:
2 RCOOH + М g → (RCOO ) 2 Mg + Н 2 ,
2 RCOOH + СаО → (RCOO ) 2 Ca + Н 2 О,
RCOOH + NaOH → RCOONa + Н 2 О,
RCOOH + NaHCO 3 → RCOONa + Н 2 О + СО 2 .
Карбоновые кислоты - слабые, поэтому сильные минеральные кислоты вытесняют их из соответствующих солей:
CH 3 COONa + HCl → СН 3 СООН + NaCl .
Соли карбоновых кислот в водных растворах гидролизованы:
СН 3 СООК + Н 2 О
![]() СН 3 СООН + КОН.
СН 3 СООН + КОН.
Отличие карбоновых кислот от минеральных заключается в возможности образования ряда функциональных производных.
3 . Образование функциональных производных карбоновых кислот. При замещении группы ОН в карбоновых кислотах различными группами (/>X ) образуются функциональные производные кислот, имеющие общую формулу R -СО- X ; здесь R означает алкильную либо арильную группу. Хотя нитрилы имеют другую общую формулу (R - CN ), обычно их также рассматривают как производные карбоновых кислот, поскольку они могут быть получены из этих кислот.
Хлорангидриды получают действием хлорида фосфора (V ) на кислоты:
R-CO-OH + РС l 5 → R-CO-Cl + РОС l 3 + HCl .
|
Соединение примеры |
|
Кислота
Этановая(уксусная) Бензойная кислота хлорангидрит кислоты
Этаноилхлорид Бензоилхлорид (ацетилхлорид) ангидрид кислоты
Этановый(уксусный) бензойный ангидрит Ангидрит сложый эфир
Этилэтаноат(этилацетат) Метилбензоат амид Этанамид(ацетамид) Бензамид Нитрил Этаннитрил Бензонитрил (ацетонитрил) |
Ангидриды образуются из карбоновых кислот при действии водоотнимающих средств:
2 R — CO — OH + Р 2 О 5 → (R — CO -) 2 O + 2НРО 3 .
Сложные эфиры образуются при нагревании кислоты со спиртом в присутствии серной кислоты (обратимая реакция этерификации):
Механизм реакции этерификации был установлен методом "меченых атомов".
Сложные эфиры можно также получить при взаимодействии хлорангидридов кислот и алкоголятов щелочных металлов:
R-CO-Cl + Na-O-R’ → R-CO-OR’ + NaCl .
Реакции хлорангидридов карбоновых кислот с аммиаком приводят к образованию амидов :
СН 3 -СО-С l + CН 3 → СН 3 -СО-CН 2 + HCl .
Кроме того, амиды могут быть получены при нагревании аммонийных солей карбоновых кислот:
При нагревании амидов в присутствии водоотнимающих средств они дегидратируются с образованием нитрилов :
| Р 2 0 5 | ||
| CH 3 — CO — NH 2 |
→ |
CH 3 — C ≡ N + Н 2 О |
Функциональные производные низших кислот — летучие жидкости. Все они легко гидролизуются с образованием исходной кислоты:
R-CO-X + Н 2 О →R-CO-OH + НХ .
В кислой среде эти реакции могут быть обратимы. Гидролиз в щелочной среде необратим и приводит к образованию солей карбоновых кислот, например:
R-CO-OR ‘ + NaOH → R-CO-ONa + R’OH.
4 . Ряд свойств карбоновых кислот обусловлен наличием углеводородного радикала. Так, при действии галогенов на кислоты в присутствии красного фосфора образуются галогензамещенные кислоты, причем на галоген замещается атом водорода при соседнем с карбоксильной группой атоме углерода (а-атоме):/>
| р кр | ||
|
СН 3 -СН 2 -СООН + Вr 2 |
→ |
СН 3 -СНВr-СООН + НВr |
Непредельные карбоновые кислоты способны к реакциям присоединения:
СН 2 =СН-СООН + Н 2 → СН 3 -СН 2 -СООН,
СН 2 =СН-СООН + С l 2 → СН 2 С l -СНС l -СООН,
СН 2 =СН-СООН + HCl → СН 2 С l -СН 2 -СООН,
СН 2 =СН-СООН + Н 2 O → НО-СН 2 -СН 2 -СООН,
Две последние реакции протекают против правила Марковникова.
Непредельные карбоновые кислоты и их производные способны к реакциям полимеризации .

5 . Окислительно-восстановительные реакции карбоновых кислот./>
Карбоновые кислоты при действии восстановителей в присутствии катализаторов способны превращаться в альдегиды, спирты и даже углеводороды:
Муравьиная кислота НСООН отличается рядом особенностей, поскольку в ее составе есть альдегидная группа:

Муравьиная кислота - сильный восстановитель и легко окисляется до СО 2 . Она дает реакцию "серебряного зеркала" :
НСООН + 2OH → 2Ag + (NH 4) 2 CO 3 + 2NH 3 + H 2 O,
или в упрощенном виде:
C Н 3 НСООН + Аg 2 О → 2Аg + СО 2 + Н 2 О.
Кроме того, муравьиная кислота окисляется хлором:
НСООН + Сl 2 → СО 2 + 2 HCl .
В атмосфере кислорода карбоновые кислоты окисляются до СО 2 и Н 2 О:
СН 3 СООН + 2О 2 → 2СО 2 + 2Н 2 О.
6 . Реакции декарбоксширования . Насыщенные незамещенные монокарбоновые кислоты из-за большой прочности связи С-С при нагревании декарбоксилируются с трудом. Для этого необходимо сплавление соли щелочного металла карбоновой кислоты со щелочью:/>
Появление электронодонорных заместителей в углеводородном радикале способствует реакции декарбоксилирования :
Двухосновные карбоновые кислоты легко отщепляют СО 2 при нагревании: